iso13485与QSR820的区别和联系
- 时间:2021-11-18作者:上海沙格医疗科技有限公司武汉分公司浏览:789
不同:ISO 13485是一个国际标准。QSR820是美国法规。一个是自愿性认证,一个是强制实施的法规。他们的结构不同。
相同:两者的条款有一定的对应关系,基本上肯定QSR820参考了13485或者反之。大约有80%的要求是相同的。如果通过了13485那搞QSR820几乎没难度,反之亦然。
上述就是为你介绍的有关iso13485与QSR820的区别和联系的内容,对此你还有什么不了解的,欢迎前来咨询我们网站,我们会有专业的人士为你讲解。
上海沙格医疗科技有限公司武汉分公司专注于IVDR,CE认证,MDR,QSR820验厂,英国UKCA认证等
词条
词条说明
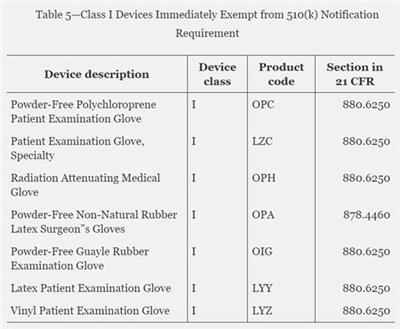
医疗器械FDA验厂(QSR820验厂)(需要名字找我):QSR820,又称21CFR820,是美国医疗器械质量管理体系法规的英文缩写,因其位于美国联邦法规(Codeof FederalRegulations)*21卷*820部分,故名21CFR820。QSR820是美国(人用)医疗器械制造商以及拟将产品销往美国的外国(人用)医疗器械制造商必须遵守的质量管理体系法规。是多数医疗器械在美国上市之前必须
ISO13485认证简介实施ISO13485国际标准给企业所带来的收益 1、ISO13485变强制性认证,日益受到欧美和中国**机构的重视,有利于*国际贸易中的技术壁垒,是取得进入国际市场的通行证;2、可提高和改善企业的管理水平,增加企业的**度;3、可提高和保证产品的质量水平,使企业获得更大的经济效益;4、有利于增强产品的竞争力,提高产品的市场占有率。5、可完善和规范企业内部工作流程与制度。上
ISO13485认证是全世界医疗设备制造商(如:美国、日本、加拿大、欧盟)较为接受的标准。这一标准包括专门针对这一行业的要求,并为诸如医疗设备、主动型医疗设备、主动型移植设备和无菌医疗设备等其他的术语做了定义。ISO13485认证支持那些生产制造或使用医疗产品和服务的企业,帮助这些企业减少不可预期的风险。该体系力图提高企业在顾客及*组织眼中的声誉。ISO134852003已正式颁布,该标准将取消
1.哪些企业需要关注UKCA的要求1)如果你有医疗器械产品销往英国市场2)如果你有医疗器械产品销往欧盟(英国以外),但是你之前的欧盟授权代表是在英国。2.如果你的医疗器械产品销往英国市场,你的应对之策包括:2.1如果是北爱尔兰市场1)继续实施CE认证,按照MDR和IVDR的要求实施;2)加贴CE标记;3)*欧盟授权代表或者英国法规责任人;4)完成产品的MHRA注册;5)产品上市销售。2.2.如果
联系方式 联系我时,请告知来自八方资源网!
公司名: 上海沙格医疗科技有限公司武汉分公司
联系人: 蒋小姐
电 话: 17717017570
手 机: 18007141921
微 信: 18007141921
地 址: 湖北武汉江汉区新华西路武汉菱角湖万达广场A区A.幢A3单元12层5号
邮 编:
相关推荐
相关阅读
1、本信息由八方资源网用户发布,八方资源网不介入任何交易过程,请自行甄别其真实性及合法性;
2、跟进信息之前,请仔细核验对方资质,所有预付定金或付款至个人账户的行为,均存在诈骗风险,请提高警惕!
- 联系方式
公司名: 上海沙格医疗科技有限公司武汉分公司
联系人: 蒋小姐
手 机: 18007141921
电 话: 17717017570
地 址: 湖北武汉江汉区新华西路武汉菱角湖万达广场A区A.幢A3单元12层5号
邮 编:
- 相关企业
- 广东亚检宏科检测有限公司
- 成都恒睿信安企业管理咨询有限公司
- 杭州临平企信商务服务工作室
- 罗普认证中心有限公司
- 傲天新盛(北京)科技有限公司
- 宁波华准检测技术有限公司
- 深圳世检检测有限公司
- 深圳市顺谨检测技术有限公司
- 天津市赛特检测有限公司
- 中标研国联(北京)认证中心
- 商家产品系列
- 产品推荐
- 资讯推荐

¥800.00



¥500.00



¥100.00

¥1.00

¥13000.00

电子后视镜陕汽Q/SQ 102084可靠性测试-专注汽车零部件DVP试验
¥99999.00