医疗器械出口澳大利亚如何分类?
- 时间:2022-11-03作者:上海角宿企业管理咨询有限公司浏览:285
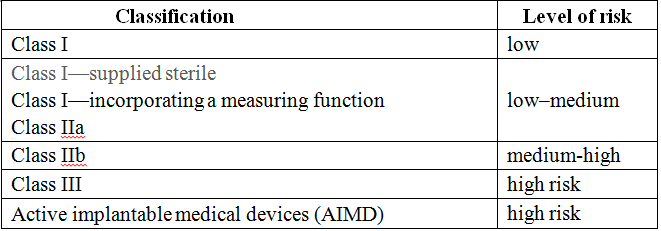
根据澳大利亚医疗用品法(Therapeutic Goods Act 1989)规定,所有在澳大利亚上市的医疗用品(药品和医疗器械)**按有关要求,向澳大利亚医疗用品管理局(Therapeutic Goods Administration, TGA)提出注册或登记申请,获得注册登记(Australian Register of Therapeutic Goods,ARTG)后才能合法上市。澳大利亚把医疗器械分为I类、Is和Im、 IIa类、IIb类、III类、AIMD,产品的分类与欧盟分类类似。
上海角宿企业管理咨询有限公司专注于FDA510(K),N95认证,TGA注册,欧代注册,欧洲自由销售证明,MDR认证,ISO13485认证,SFDA注册,FDA注册等, 欢迎致电 17802157742
词条
词条说明
当您不再持有足够的证据时TGA要求:当您没有或无法保持足够的安全和性能证据时(例如,关于以前无法预见的危险的新证据变得可用),您必须修改您的预期目的以缩小范围,修改您的使用说明等。如果您发现您的设备存在重大且不可接受的安全问题,您必须停止供应、进行召回或将您的设备从 ARTG 中移除。您可以持有的证据类型您可以使用一系列数据作为客观证据来表明您的设备符合这些原则。下面的列表包括一些建议。请注意,此
中国药品或保健品想在澳大利亚获得TGA认证前,TGA要求在注册或注册产品在澳大利亚必须确认其生产设施和制造工艺符合澳大利亚GMP要求,即所谓的“GMP清理”流程,即GMP审核流程。因此,为了能够在澳大利亚销售药品,必须通过Australian-TGA现场检查获得符合GMP标准的批准。注册文件审核的核心是产品是否符合“安全,有效,高质量”的要求。一旦GMP检查和注册审查符合要求,TGA可以批准该产品
1、新研制的医疗器械如何确定产品管理类别?答:根据《医疗器械注册与备案管理办法》*六十四条:对新研制的尚未列入分类目录的医疗器械,申请人可以直接申请第三类医疗器械产品注册,也可以依据分类规则判断产品类别并向国家药品监督管理局申请类别确认后,申请产品注册或者进行产品备案。2、医疗器械(不含体外诊断试剂)**注册申请时,应提交哪些资料?答:请参照《国家药监局关于公布医疗器械注册申报资料要求和批准证明文
为了确保医疗器械的安全和有效性,新加坡将医疗器械产品分为A、B、C、D等4类,根据风险等级进行管理和注册。A类医疗器械注册申请步骤:1. 提交申请:申请公司需要填写并提交完整的注册申请表格,包括产品的详细信息、技术规格和相关证书等。2. 筛选:主管部门将对申请材料进行初步筛选,确保符合注册要求。3. 评审:经过初步筛选的申请将进行详细评审,包括对产品的性能、安全性和有效性进行评估。4. 主管部门作
联系方式 联系我时,请告知来自八方资源网!
公司名: 上海角宿企业管理咨询有限公司
联系人: 杨经理
电 话:
手 机: 17802157742
微 信: 17802157742
地 址: 上海浦东申港申港大道133号609
邮 编:
网 址: bys0613.b2b168.com
相关推荐
相关阅读
1、本信息由八方资源网用户发布,八方资源网不介入任何交易过程,请自行甄别其真实性及合法性;
2、跟进信息之前,请仔细核验对方资质,所有预付定金或付款至个人账户的行为,均存在诈骗风险,请提高警惕!
- 联系方式
公司名: 上海角宿企业管理咨询有限公司
联系人: 杨经理
手 机: 17802157742
电 话:
地 址: 上海浦东申港申港大道133号609
邮 编:
网 址: bys0613.b2b168.com
- 相关企业
- 江苏凡睿管理咨询有限公司
- 湖北华思企业管理有限公司
- 北京宏易管理咨询有限公司
- 重庆博视知识产权服务有限公司
- 青岛刘小帮企业管理咨询有限公司
- 广西英达思企业管理咨询有限公司
- 河南省新起点企业管理咨询有限公司
- 成都遇上良缘婚姻服务有限公司
- 广东励信知识产权服务有限公司
- 广东华智天诚管理顾问有限公司
- 商家产品系列
- 产品推荐
- 资讯推荐


¥1000.00


¥500.00



血压计FDA器械注册的测试标准-SPICA INSIGHTS
¥30000.00

¥2000.00























